Nozokomiální pneumonie je nejčastější a nejzávažnější nozokomiální infekcí, z níž ventilátorová pneumonie (VAP) představuje 40 %. VAP způsobená refrakterními patogeny je stále obtížným klinickým problémem. Pokyny již léta doporučují řadu intervencí (jako je cílená sedace, elevace hlavy) k prevenci VAP, ale VAP se vyskytuje až u 40 % pacientů s tracheální intubací, což vede k delším pobytům v nemocnici, zvýšenému užívání antibiotik a úmrtí. Lidé neustále hledají účinnější preventivní opatření.
Ventilátorová pneumonie (VAP) je nově vznikající pneumonie, která se rozvíjí 48 hodin po tracheální intubaci a je nejčastější a nejsmrtelnější nozokomiální infekcí na jednotce intenzivní péče (JIP). Pokyny Americké společnosti pro infekční nemoci z roku 2016 odlišují VAP od definice nozokomiální pneumonie (HAP) (HAP označuje pouze pneumonii, která se vyskytuje po hospitalizaci bez tracheální kanyly a nesouvisí s mechanickou ventilací; VAP je pneumonie po tracheální intubaci a mechanické ventilaci) a Evropská společnost a Čína se domnívají, že VAP je stále zvláštním typem HAP [1-3].
U pacientů podstupujících mechanickou ventilaci se incidence VAP pohybuje od 9 % do 27 %, úmrtnost se odhaduje na 13 % a může vést ke zvýšenému systémovému užívání antibiotik, prodloužené mechanické ventilaci, prodloužené pobytu na JIP a zvýšeným nákladům [4-6]. HAP/VAP u pacientů bez imunodeficience je obvykle způsobena bakteriální infekcí a distribuce běžných patogenů a jejich charakteristiky rezistence se liší v závislosti na regionu, nemocniční třídě, populaci pacientů a expozici antibiotikům a mění se v průběhu času. Pseudomonas aeruginosa dominovala patogenům souvisejícím s VAP v Evropě a Americe, zatímco v Číně bylo v terciárních nemocnicích izolováno více Acinetobacter baumannii. Třetina až polovina všech úmrtí souvisejících s VAP je přímo způsobena infekcí, přičemž úmrtnost případů způsobených Pseudomonas aeruginosa a acinetobacterem je vyšší [7,8].
Vzhledem k silné heterogenitě ventilační pneumonie (VAP) je diagnostická specificita jejích klinických projevů, zobrazovacích a laboratorních testů nízká a rozsah diferenciální diagnostiky je široký, což ztěžuje včasnou diagnostiku VAP. Zároveň bakteriální rezistence představuje vážnou výzvu pro léčbu VAP. Odhaduje se, že riziko vzniku VAP je 3 %/den během prvních 5 dnů používání mechanické ventilace, 2 %/den mezi 5. a 10. dnem a 1 %/den po zbytek doby. Vrchol incidence obvykle nastává po 7 dnech ventilace, takže existuje okno, ve kterém lze infekci včas zabránit [9,10]. Mnoho studií se zabývalo prevencí VAP, ale navzdory desetiletím výzkumu a pokusům o prevenci VAP (jako je vyhýbání se intubaci, prevence reintubace, snížení sedace, zvednutí hlavy postele o 30° až 45° a péče o ústní dutinu) se incidence nezdá snížila a související lékařská zátěž zůstává velmi vysoká.
Inhalační antibiotika se používají k léčbě chronických infekcí dýchacích cest od 40. let 20. století. Protože mohou maximalizovat doručení léků do cílového místa infekce (tj. dýchacích cest) a snížit systémové vedlejší účinky, prokázaly dobrou aplikační hodnotu u řady onemocnění. Inhalační antibiotika jsou nyní schválena americkým Úřadem pro kontrolu potravin a léčiv (FDA) a Evropskou agenturou pro léčivé přípravky (EMA) pro použití u cystické fibrózy. Inhalační antibiotika mohou významně snížit bakteriální zátěž a frekvenci exacerbací bronchiektázií, aniž by zvýšila celkové nežádoucí účinky, a současné směrnice je uznávají jako léčbu první volby u pacientů s infekcí Pseudomonas aeruginosa a častými exacerbacemi. Inhalační antibiotika lze také použít jako adjuvantní nebo profylaktické léky během perioperačního období transplantace plic [11,12]. V amerických směrnicích VAP z roku 2016 však odborníci postrádali důvěru v účinnost adjuvantních inhalačních antibiotik kvůli nedostatku velkých randomizovaných kontrolovaných studií. Studie fáze 3 (INHALE) publikovaná v roce 2020 rovněž nepřinesla pozitivní výsledky (inhalace amikacinem asistovaná intravenózní antibiotika u gramnegativních bakteriálních infekcí způsobených pacienty s VAP, dvojitě zaslepená, randomizovaná, placebem kontrolovaná studie účinnosti fáze 3, celkem 807 pacientů, systémová medikace + asistovaná inhalace amikacinu po dobu 10 dnů).
V této souvislosti tým vedený výzkumníky z Regionálního univerzitního nemocničního centra v Tours (CHRU) ve Francii zvolil odlišnou výzkumnou strategii a provedl multicentrickou, dvojitě zaslepenou, randomizovanou kontrolovanou studii účinnosti (AMIKINHAL), kterou inicioval výzkumník. Inhalační amikacin nebo placebo v prevenci VAP byly porovnávány u 19 jednotek intenzivní péče ve Francii [13].
Celkem 847 dospělých pacientů s invazivní mechanickou ventilací v délce trvání 72 až 96 hodin bylo náhodně zařazeno v poměru 1:1 do skupiny s inhalací amikacinu (N=417,20 mg/kg ideální tělesné hmotnosti, QD) nebo inhalací placeba (N=430, 0,9% ekvivalent chloridu sodného) po dobu 3 dnů. Primárním cílovým parametrem byla první epizoda VAP od začátku randomizovaného zařazení do 28. dne.
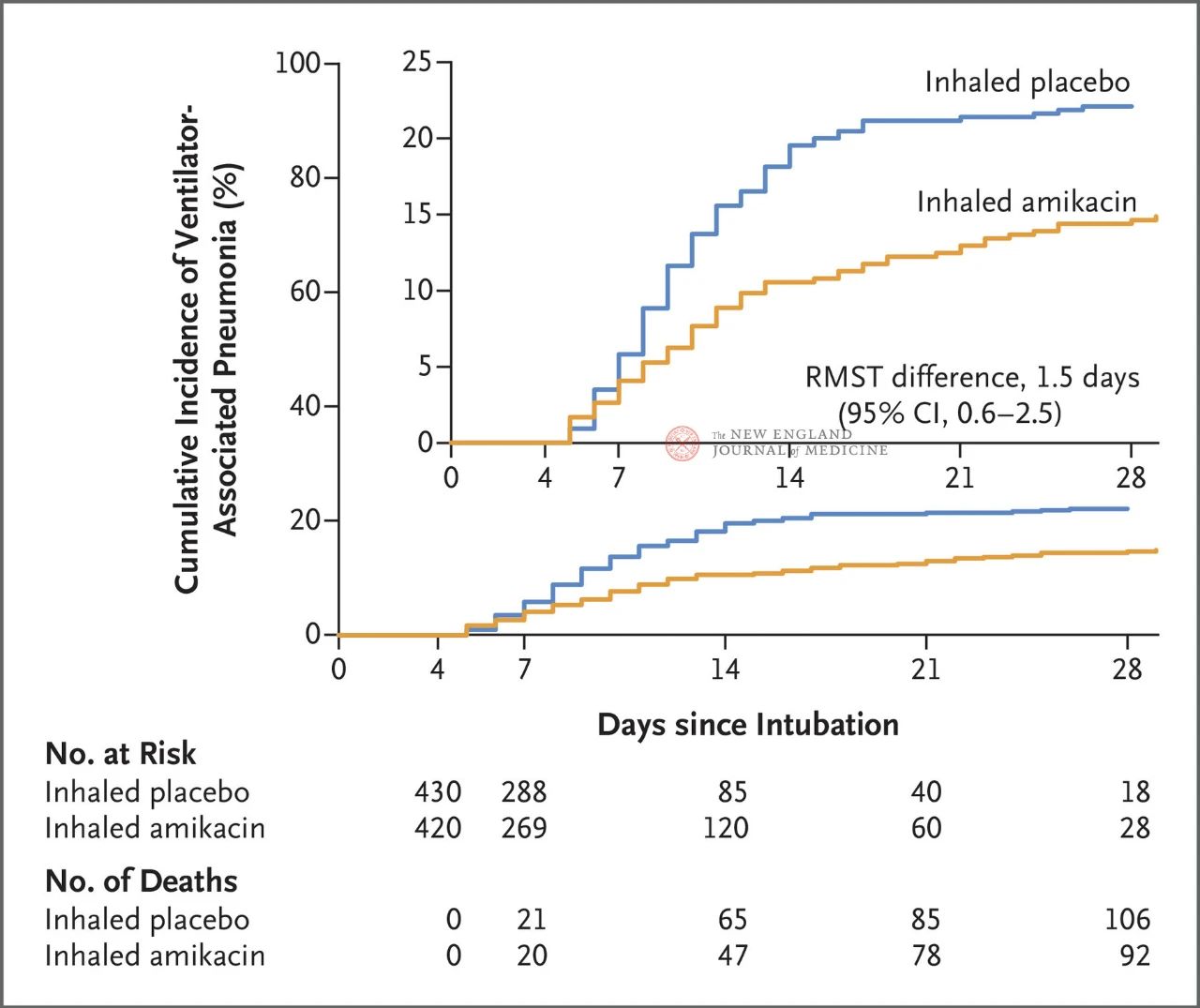
Výsledky studie ukázaly, že po 28 dnech se u 62 pacientů (15 %) ve skupině s amikacinem vyvinula VAP a u 95 pacientů (22 %) ve skupině s placebem se vyvinula VAP (omezený průměrný rozdíl v přežití pro VAP byl 1,5 dne; 95% interval spolehlivosti, 0,6–2,5; P = 0,004).
Z hlediska bezpečnosti se u sedmi pacientů (1,7 %) ve skupině s amikacinem a u čtyř pacientů (0,9 %) ve skupině s placebem vyskytly závažné nežádoucí účinky související se studií. Mezi těmi, kteří při randomizaci neměli akutní poškození ledvin, mělo 11 pacientů (4 %) ve skupině s amikacinem a 24 pacientů (8 %) ve skupině s placebem akutní poškození ledvin 28. den (HR 0,47; 95% CI 0,23–0,96).
Klinická studie měla tři hlavní body. Zaprvé, z hlediska designu studie, studie AMIKINHAL čerpá ze studie IASIS (randomizovaná, dvojitě zaslepená, placebem kontrolovaná, paralelní studie fáze 2 zahrnující 143 pacientů). Pro vyhodnocení bezpečnosti a účinnosti inhalační léčby amikacinem a fosfomycinem v systémové léčbě infekcí gramnegativními bakteriemi způsobených ventilační péčí (VAP) a studie INHALE, která skončila s negativními výsledky, se zaměřila na prevenci VAP a dosáhla relativně dobrých výsledků. Vzhledem k charakteristikám vysoké úmrtnosti a dlouhé hospitalizace u pacientů s mechanickou ventilací a VAP, pokud inhalace amikacinu může dosáhnout významně odlišných výsledků ve snižování úmrtnosti a hospitalizace u těchto pacientů, bude pro klinickou praxi cennější. Vzhledem k heterogenitě pozdní léčby a péče u každého pacienta a každého centra však existuje řada matoucích faktorů, které mohou studii ovlivnit, takže může být také obtížné získat pozitivní výsledek, který lze připsat inhalačním antibiotikům. Úspěšná klinická studie proto vyžaduje nejen vynikající design studie, ale také výběr vhodných primárních cílových parametrů.
Za druhé, ačkoli aminoglykosidová antibiotika nejsou v různých směrnicích pro VAP doporučována jako samostatný lék, mohou aminoglykosidová antibiotika pokrýt běžné patogeny u pacientů s VAP (včetně Pseudomonas aeruginosa, acinetobacter atd.), a to díky jejich omezené absorpci v plicních epiteliálních buňkách, vysoké koncentraci v místě infekce a nízké systémové toxicitě. Aminoglykosidová antibiotika jsou mezi inhalačními antibiotiky široce upřednostňována. Tato práce je v souladu s komplexním odhadem velikosti účinku intratracheálního podání gentamicinu v malých vzorcích publikovaným dříve, který společně demonstruje účinek inhalačních aminoglykosidových antibiotik v prevenci VAP. Je třeba také poznamenat, že většina placebových kontrol vybraných ve studiích týkajících se inhalačních antibiotik je fyziologický roztok. Vzhledem k tomu, že atomizovaná inhalace fyziologického roztoku sama o sobě může hrát určitou roli v ředění sputa a napomáhat expektoranci, může fyziologický roztok způsobit určité interference s analýzou výsledků studie, což by mělo být ve studii komplexně zváženo.
Dále je důležitá lokální adaptace léků HAP/VAP, stejně jako antibiotická profylaxe. Zároveň, bez ohledu na délku intubace, je ekologie místní JIP nejdůležitějším rizikovým faktorem pro infekci multirezistentními bakteriemi. Empirická léčba by se proto měla co nejvíce odvolávat na mikrobiologická data místních nemocnic a neměla by se slepě odvolávat na směrnice nebo zkušenosti terciárních nemocnic. Zároveň kriticky nemocní pacienti vyžadující mechanickou ventilaci trpí často multisystémovými onemocněními a při kombinovaném působení více faktorů, jako je stresový stav, může dojít také k fenoménu přeslechů střevních mikrobů do plic. Vysoká heterogenita onemocnění způsobená vnitřní a vnější superpozicí také určuje, že rozsáhlá klinická propagace každého nového zákroku je ještě dlouhou cestou.
Čas zveřejnění: 2. prosince 2023