Alzheimerova choroba, nejčastější případ starších lidí, trápí většinu lidí.
Jednou z výzev v léčbě Alzheimerovy choroby je, že dodávání terapeutických léků do mozkové tkáně je omezeno hematoencefalickou bariérou. Studie zjistila, že nízkointenzivní fokusovaný ultrazvuk s magnetickou rezonancí může reverzibilně otevřít hematoencefalickou bariéru u pacientů s Alzheimerovou chorobou nebo jinými neurologickými poruchami, včetně Parkinsonovy choroby, mozkových nádorů a amyotrofické laterální sklerózy.
Nedávná malá studie zaměřená na ověření konceptu v Rockefellerově institutu pro neurovědy na Západní Virginské univerzitě ukázala, že pacienti s Alzheimerovou chorobou, kteří dostávali infuzi adukanumabu v kombinaci s fokusovaným ultrazvukem, dočasně otevřeli hematoencefalickou bariéru a významně snížili množství mozkového amyloidu beta (Aβ) na straně studie. Výzkum by mohl otevřít nové možnosti léčby mozkových poruch.
Hematoencefalická bariéra chrání mozek před škodlivými látkami a zároveň umožňuje průchod esenciálních živin. Hematoencefalická bariéra však také brání dodávání terapeutických léků do mozku, což je problém, který je obzvláště akutní při léčbě Alzheimerovy choroby. S tím, jak svět stárne, počet lidí s Alzheimerovou chorobou rok od roku roste a možnosti léčby jsou omezené, což představuje velkou zátěž pro zdravotní péči. Aducanumab je monoklonální protilátka vázající se na amyloid beta (Aβ), která byla schválena americkým Úřadem pro kontrolu potravin a léčiv (FDA) pro léčbu Alzheimerovy choroby, ale její průnik hematoencefalickou bariérou je omezený.
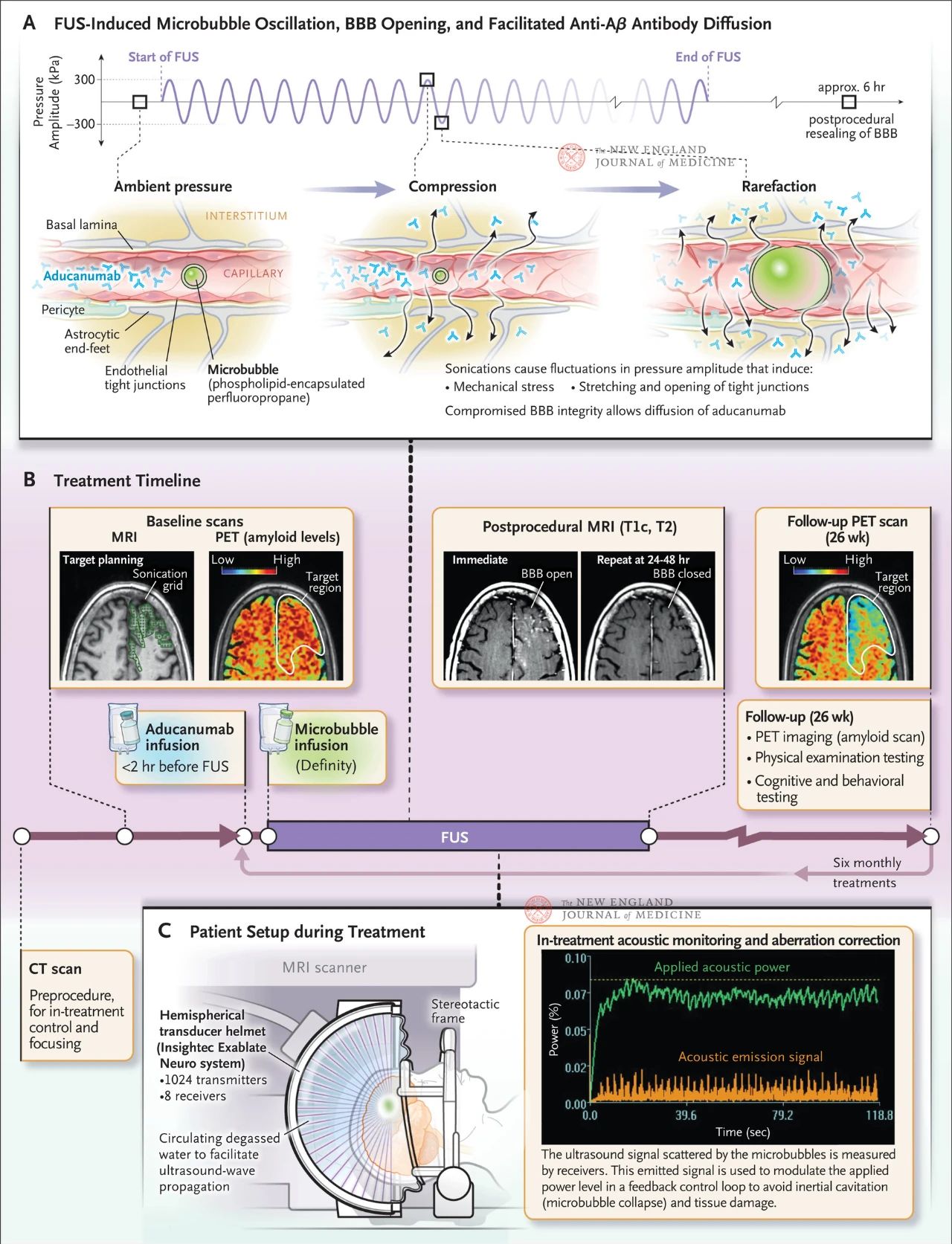
Fokusovaný ultrazvuk produkuje mechanické vlny, které indukují oscilace mezi kompresí a ředěním. Po injekčním podání do krve a vystavení ultrazvukovému poli se bubliny stlačují a roztahují více než okolní tkáň a krev. Tyto oscilace vytvářejí mechanické namáhání stěny cév, což způsobuje natažení a otevření těsných spojení mezi endotelovými buňkami (obrázek níže). V důsledku toho je narušena integrita hematoencefalické bariéry, což umožňuje molekulám difundovat do mozku. Hematoencefalická bariéra se sama zahojí přibližně za šest hodin.
Obrázek ukazuje vliv směrového ultrazvuku na kapilární stěny, když jsou v cévách přítomny bublinky o velikosti mikrometrů. Vzhledem k vysoké stlačitelnosti plynu se bublinky smršťují a roztahují více než okolní tkáň, což způsobuje mechanické namáhání endotelových buněk. Tento proces způsobuje otevírání těsných spojení a může také způsobit odpadávání zakončení astrocytů ze stěny cév, což narušuje integritu hematoencefalické bariéry a podporuje difúzi protilátek. Endotelové buňky vystavené fokusovanému ultrazvuku navíc zvýšily svou aktivní vakuolární transportní aktivitu a potlačily funkci efluxní pumpy, čímž se snížilo odbourávání protilátek z mozku. Obrázek B ukazuje léčebný plán, který zahrnuje počítačovou tomografii (CT) a magnetickou rezonanci (MRI) pro vytvoření plánu ultrazvukové léčby, pozitronovou emisní tomografii (PET) s 18F-flubitabanem na začátku léčby, infuzi protilátek před fokusovanou ultrazvukovou léčbou a mikrovezikulární infuzi během léčby a akustické monitorování ultrazvukových signálů s mikrovezikulárním rozptylem používaných ke kontrole léčby. Snímky získané po fokusované ultrazvukové léčbě zahrnovaly T1-váženou MRI s kontrastem, která ukázala, že hematoencefalická bariéra byla v oblasti ošetřené ultrazvukem otevřená. Snímky stejné oblasti po 24 až 48 hodinách léčby fokusovaným ultrazvukem ukázaly úplné zhojení hematoencefalické bariéry. PET vyšetření s 18F-flubitabanem během následného sledování u jednoho z pacientů o 26 týdnů později ukázalo snížené hladiny Aβ v mozku po léčbě. Obrázek C ukazuje nastavení fokusovaného ultrazvuku s magnetickou rezonancí během léčby. Hemisférická převodní přilba obsahuje více než 1 000 ultrazvukových zdrojů, které se sbíhají do jediného ohniska v mozku pomocí navádění z magnetické rezonance v reálném čase.
V roce 2001 bylo ve studiích na zvířatech poprvé prokázáno, že fokusovaný ultrazvuk indukuje otevření hematoencefalické bariéry, a následné preklinické studie ukázaly, že fokusovaný ultrazvuk může zlepšit podávání a účinnost léků. Od té doby se zjistilo, že fokusovaný ultrazvuk může bezpečně otevřít hematoencefalickou bariéru u pacientů s Alzheimerovou chorobou, kteří neužívají léky, a může také doručit protilátky proti mozkovým metastázám rakoviny prsu.
Proces podávání mikrobublin
Mikrobubliny jsou ultrazvuková kontrastní látka, která se obvykle používá k pozorování průtoku krve a cév v ultrazvukové diagnostice. Během ultrazvukové terapie byla intravenózně injekčně podána suspenze oktafluoropropanu s nepyrogenními bublinami potaženými fosfolipidy (obrázek 1B). Mikrobubliny jsou vysoce polydisperzní, s průměry od menších než 1 μm do více než 10 μm. Oktafluoropropan je stabilní plyn, který se nemetabolizuje a může být vylučován plícemi. Lipidová schránka, která bubliny obaluje a stabilizuje, se skládá ze tří přirozených lidských lipidů, které jsou metabolizovány podobným způsobem jako endogenní fosfolipidy.
Generování fokusovaného ultrazvuku
Fokusovaný ultrazvuk je generován hemisférickou měnicí přilbou, která obklopuje hlavu pacienta (obrázek 1C). Přilba je vybavena 1024 nezávisle řízenými ultrazvukovými zdroji, které jsou přirozeně zaostřeny ve středu hemisféry. Tyto ultrazvukové zdroje jsou poháněny sinusovým radiofrekvenčním napětím a emitují ultrazvukové vlny vedené magnetickou rezonancí. Pacient má nasazenou přilbu a kolem hlavy cirkuluje odplyněná voda, která usnadňuje přenos ultrazvuku. Ultrazvuk prochází kůží a lebkou do cílového mozku.
Změny tloušťky a hustoty lebky ovlivní šíření ultrazvuku, což má za následek mírně odlišnou dobu, než ultrazvuk dosáhne léze. Toto zkreslení lze korigovat získáním dat z počítačové tomografie s vysokým rozlišením, která umožní získat informace o tvaru, tloušťce a hustotě lebky. Počítačový simulační model dokáže vypočítat kompenzovaný fázový posun každého budicího signálu a obnovit tak ostré zaostření. Řízením fáze RF signálu lze ultrazvuk elektronicky zaostřit a umístit tak, aby pokrýval velké množství tkáně, aniž by se musel pohybovat zdrojovým polem ultrazvuku. Umístění cílové tkáně se určuje magnetickou rezonancí hlavy s nasazenou helmou. Cílový objem je vyplněn trojrozměrnou mřížkou ultrazvukových kotevních bodů, které v každém kotevním bodě emitují ultrazvukové vlny po dobu 5–10 ms, opakovaně každé 3 sekundy. Ultrazvukový výkon se postupně zvyšuje, dokud není detekován požadovaný signál rozptylu bublin, a poté se udržuje po dobu 120 sekund. Tento proces se opakuje na dalších sítích, dokud není cílový objem zcela pokryt.
Otevření hematoencefalické bariéry vyžaduje, aby amplituda zvukových vln překročila určitou prahovou hodnotu, za níž se propustnost bariéry zvyšuje se zvyšující se amplitudou tlaku, dokud nedojde k poškození tkáně, které se projevuje jako exosmóza erytrocytů, krvácení, apoptóza a nekróza, což vše je často spojeno s kolapsem bubliny (tzv. inerciální kavitace). Prahová hodnota závisí na velikosti mikrobublin a materiálu obalu. Detekcí a interpretací ultrazvukových signálů rozptýlených mikrobublinami lze udržet expozici v bezpečném rozmezí.
Po ultrazvukovém ošetření byla použita T1-vážená magnetická rezonance s kontrastní látkou k určení, zda je hematoencefalická bariéra v cílovém místě otevřená, a T2-vážené snímky byly použity k potvrzení, zda došlo k extravazaci nebo krvácení. Tato pozorování poskytují vodítko pro úpravu další léčby, pokud je to nutné.
Hodnocení a vyhlídky na terapeutický účinek
Vědci kvantifikovali vliv léčby na zátěž mozku Aβ porovnáním pozitronové emisní tomografie s 18F-flubitabanem před a po léčbě, aby posoudili rozdíl v objemu Aβ mezi ošetřenou oblastí a podobnou oblastí na opačné straně. Předchozí výzkum stejného týmu ukázal, že pouhé zaostření ultrazvuku může mírně snížit hladiny Aβ. Snížení pozorované v této studii bylo ještě větší než v předchozích studiích.
V budoucnu bude rozšíření léčby na obě strany mozku klíčové pro vyhodnocení její účinnosti při zpomalení progrese onemocnění. Kromě toho je zapotřebí dalšího výzkumu k určení dlouhodobé bezpečnosti a účinnosti a pro širší dostupnost je nutné vyvinout cenově dostupné terapeutické přístroje, které nebudou závislé na online MRI vyšetření. Zjištění však vyvolala optimismus, že léčba a léky, které odstraňují Aβ, by nakonec mohly zpomalit progresi Alzheimerovy choroby.
Čas zveřejnění: 6. ledna 2024