V dnešní době se nealkoholické ztučnění jater (NAFLD) stalo hlavní příčinou chronického onemocnění jater v Číně a dokonce i ve světě. Spektrum onemocnění zahrnuje jednoduchou jaterní steatohepatitidu, nealkoholickou steatohepatitidu (NASH) a související cirhózu a rakovinu jater. NASH je charakterizován nadměrnou akumulací tuku v hepatocytech a indukovaným poškozením buněk a zánětem, s jaterní fibrózou nebo bez ní. Závažnost jaterní fibrózy u pacientů s NASH je úzce spojena se špatnou prognózou jater (cirhóza a její komplikace a hepatocelulární karcinom), kardiovaskulárními příhodami, extrahepatálními malignitami a úmrtím ze všech příčin. NASH může nepříznivě ovlivnit kvalitu života pacientů; nicméně dosud nebyly schváleny žádné léky ani terapie k léčbě NASH.
Nedávná studie (ENLIVEN) publikovaná v časopise New England Journal of Medicine (NEJM) ukázala, že pegozafermin zlepšil jak fibrózu jater, tak zánět jater u pacientů s NASH bez cirhózy potvrzenou biopsií.
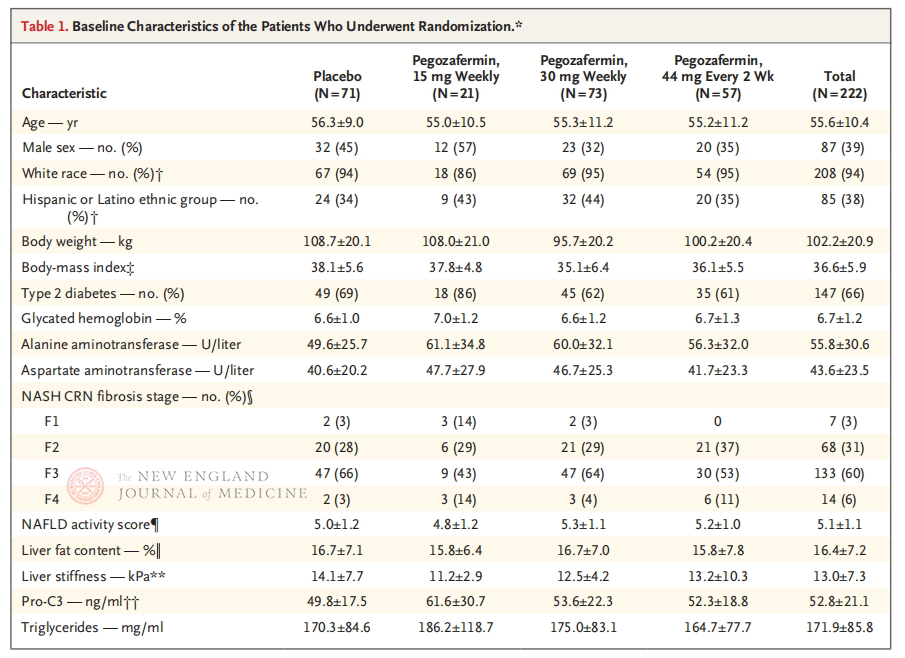
Multicentrická, randomizovaná, dvojitě zaslepená, placebem kontrolovaná klinická studie fáze 2b, kterou provedl profesor Rohit Loomba a jeho klinický tým na Lékařské fakultě Kalifornské univerzity v San Diegu, zahrnovala 222 pacientů s biopsií potvrzenou NASH ve stádiu F2-3 v období od 28. září 2021 do 15. srpna 2022. Pacienti byli náhodně zařazeni do skupiny s pegozaferminem (subkutánní injekce, 15 mg nebo 30 mg jednou týdně, nebo 44 mg jednou za 2 týdny) nebo do skupiny s placebem (jednou týdně nebo jednou za 2 týdny). Primárními cílovými parametry bylo zlepšení fibrózy ≥ 1. stádia a žádná progrese NASH. NASH ustoupila bez fibrotické progrese. Studie provedla také hodnocení bezpečnosti.
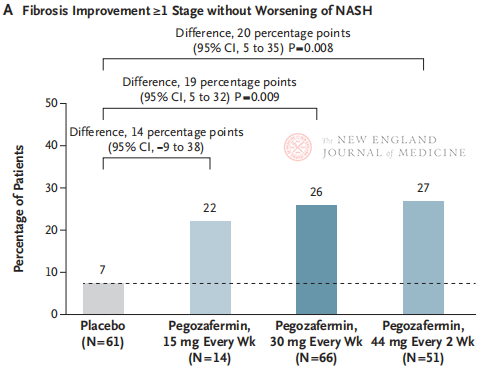
Po 24 týdnech léčby byl podíl pacientů se zlepšením fibrózy ≥ 1. stupně a bez zhoršení NASH a podíl pacientů s regresí NASH a bez zhoršení fibrózy významně vyšší ve třech skupinách s dávkou pegozaferminu než ve skupině s placebem, s významnějšími rozdíly u pacientů léčených dávkou 44 mg jednou za dva týdny nebo 30 mg jednou týdně. Z hlediska bezpečnosti byl pegozafermin podobný placebu. Nejčastějšími nežádoucími účinky spojenými s léčbou pegozaferminem byly nevolnost, průjem a erytém v místě injekce. V této studii fáze 2b předběžné výsledky naznačují, že léčba pegozaferminem zlepšuje jaterní fibrózu.
Pegozafermin, použitý v této studii, je dlouhodobě působící glykolovaný analog lidského fibroblastového růstového faktoru 21 (FGF21). FGF21 je endogenní metabolický hormon vylučovaný játry, který hraje roli v regulaci metabolismu lipidů a glukózy. Předchozí studie prokázaly, že FGF21 má terapeutické účinky na pacienty s NASH zvýšením citlivosti jater na inzulín, stimulací oxidace mastných kyselin a inhibicí lipogeneze. Krátký poločas rozpadu přirozeného FGF21 (přibližně 2 hodiny) však omezuje jeho použití v klinické léčbě NASH. Pegozafermin využívá technologii glykosylované pegylace k prodloužení poločasu rozpadu přirozeného FGF21 a optimalizaci jeho biologické aktivity.
Kromě pozitivních výsledků této klinické studie fáze 2b ukázala další nedávná studie publikovaná v časopise Nature Medicine (ENTRIGUE), že pegozafermin také významně snižuje triglyceridy, non-HDL cholesterol, apolipoprotein B a jaterní steatózu u pacientů s těžkou hypertriglyceridemií, což může mít pozitivní vliv na snížení rizika kardiovaskulárních příhod u pacientů s NASH.
Tyto studie naznačují, že pegozafermin, jakožto endogenní metabolický hormon, může pacientům s NASH poskytnout řadu metabolických výhod, zejména proto, že NASH by v budoucnu mohl být přejmenován na metabolicky asociované ztučnění jater. Díky těmto výsledkům se jedná o velmi důležitý potenciální lék pro léčbu NASH. Zároveň tyto pozitivní výsledky studie podpoří zařazení pegozaferminu do fáze 3 klinických studií.
Přestože jak léčba pegozaferminem v dávce 44 mg jednou za dva týdny, tak i léčba pegozaferminem v dávce 30 mg jednou týdně dosáhla histologického primárního cílového parametru studie, délka léčby v této studii byla pouze 24 týdnů a míra dodržování léčby ve skupině s placebem byla pouze 7 %, což bylo významně méně než výsledky předchozích klinických studií trvajících 48 týdnů. Jsou rozdíly a bezpečnost stejné? Vzhledem k heterogenitě NASH jsou v budoucnu zapotřebí rozsáhlejší, multicentrické, mezinárodní klinické studie, které by zahrnovaly větší populace pacientů a prodloužily dobu léčby, aby se lépe vyhodnotila účinnost a bezpečnost léku.
Čas zveřejnění: 16. září 2023