Kachexie je systémové onemocnění charakterizované úbytkem hmotnosti, atrofií svalové a tukové tkáně a systémovým zánětem. Kachexie je jednou z hlavních komplikací a příčin úmrtí u pacientů s rakovinou. Odhaduje se, že výskyt kachexie u pacientů s rakovinou může dosáhnout 25 % až 70 % a každoročně trpí kachexií přibližně 9 milionů lidí na celém světě, z nichž 80 % pravděpodobně zemře do jednoho roku od stanovení diagnózy. Kachexie navíc významně ovlivňuje kvalitu života pacientů a zhoršuje toxicitu související s léčbou.
Účinná intervence kachexie má velký význam pro zlepšení kvality života a prognózy pacientů s rakovinou. Navzdory určitému pokroku ve studiu patofyziologických mechanismů kachexie je však mnoho léků vyvinutých na základě možných mechanismů pouze částečně účinných nebo neúčinných. V současné době neexistuje žádná účinná léčba schválená americkým Úřadem pro kontrolu potravin a léčiv (FDA).
Kachexie (syndrom chřadnutí) je velmi častá u pacientů s mnoha typy rakoviny a často vede k úbytku hmotnosti, úbytku svalové hmoty, snížené kvalitě života, zhoršené funkci a zkrácenému přežití. Podle mezinárodně uznávaných standardů je tento multifaktoriální syndrom definován jako index tělesné hmotnosti (BMI, hmotnost [kg] dělená výškou [m] na druhou) menší než 20 nebo u pacientů se sarkopenií úbytek hmotnosti o více než 5 % za šest měsíců nebo úbytek hmotnosti o více než 2 %. V současné době nebyly ve Spojených státech ani v Evropě schváleny žádné léky specificky určené k léčbě rakovinné kachexie, což má za následek omezené možnosti léčby.
Nedávné směrnice doporučující nízké dávky olanzapinu ke zlepšení chuti k jídlu a hmotnosti u pacientů s pokročilým karcinomem jsou z velké části založeny na výsledcích studie provedené v jednom centru. Kromě toho může krátkodobé užívání analogů progesteronu nebo glukokortikoidů přinést omezené výhody, ale existuje riziko nežádoucích vedlejších účinků (jako je užívání progesteronu spojené s tromboembolickými příhodami). Klinické studie jiných léků neprokázaly dostatečnou účinnost k získání schválení regulačními orgány. Ačkoli anamorin (perorální verze peptidů uvolňujících růstový hormon) byl v Japonsku schválen k léčbě rakovinné kachexie, lék pouze do určité míry zvýšil složení těla, nezlepšil sílu úchopu a nakonec nebyl schválen americkým Úřadem pro kontrolu potravin a léčiv (FDA). Existuje naléhavá potřeba bezpečné, účinné a cílené léčby rakovinné kachexie.
Růstový diferenciační faktor 15 (GDF-15) je stresem indukovaný cytokin, který se váže na protein podobný receptoru alfa (GFRAL) z rodiny neurotrofických faktorů odvozených od glií v zadní části mozku. Dráha GDF-15-GFRAL byla identifikována jako hlavní regulátor anorexie a regulace hmotnosti a hraje roli v patogenezi kachexie. Na zvířecích modelech může GDF-15 indukovat kachexii a inhibice GDF-15 může tento příznak zmírnit. Kromě toho jsou zvýšené hladiny GDF-15 u pacientů s rakovinou spojeny se snížením tělesné hmotnosti a hmotnosti kosterního svalstva, snížením síly a zkráceným přežitím, což podtrhuje hodnotu GDF-15 jako potenciálního terapeutického cíle.
Ponsegromab (PF-06946860) je vysoce selektivní humanizovaná monoklonální protilátka schopná vazby na cirkulující GDF-15, čímž inhibuje jeho interakci s receptorem GFRAL. V malé otevřené studii fáze 1b bylo 10 pacientů s rakovinnou kachexií a zvýšenými hladinami cirkulujícího GDF-15 léčeno ponsegromabem a došlo u nich ke zlepšení hmotnosti, chuti k jídlu a fyzické aktivity, zatímco hladiny GDF-15 v séru byly inhibovány a nežádoucí účinky byly nízké. Na základě toho jsme provedli klinickou studii fáze 2 s cílem vyhodnotit bezpečnost a účinnost ponsegromabu u pacientů s rakovinnou kachexií se zvýšenými hladinami cirkulujícího GDF-15 ve srovnání s placebem, abychom otestovali hypotézu, že GDF-15 je primární patogenezí onemocnění.
Studie zahrnovala dospělé pacienty s kachexií spojenou s rakovinou (nemalobuněčný karcinom plic, karcinom slinivky břišní nebo kolorektální karcinom) s hladinou GDF-15 v séru alespoň 1500 pg/ml, skóre fitness statusu dle Eastern Tumor Consortium (ECOG) ≤3 a očekávanou délkou života alespoň 4 měsíce.
Zařazení pacienti byli náhodně rozděleni do skupin, kterým byly subkutánně aplikovány 3 dávky ponsegromabu 100 mg, 200 mg nebo 400 mg nebo placeba, nebo placeba, každé 4 týdny v poměru 1:1:1. Primárním cílovým parametrem byla změna tělesné hmotnosti ve srovnání s výchozím stavem po 12 týdnech. Klíčovým sekundárním cílovým parametrem byla změna skóre FAACT-ACS (anorexia cachexia Sub-Scale) oproti výchozímu stavu, což je hodnocení terapeutické funkce u anorexické kachexie. Další sekundární cílové parametry zahrnovaly skóre deníku symptomů kachexie spojené s rakovinou, výchozí změny fyzické aktivity a cílové parametry chůze měřené pomocí nositelných digitálních zdravotnických zařízení. Minimální požadavky na dobu nošení jsou specifikovány předem. Posouzení bezpečnosti zahrnovalo počet nežádoucích účinků během léčby, výsledky laboratorních testů, vitální funkce a elektrokardiogramy. Explorativní cílové parametry zahrnovaly výchozí změny indexu bederního kosterního svalstva (plocha kosterního svalstva dělená druhou mocninou výšky) spojené se systémovým kosterním svalstvem.
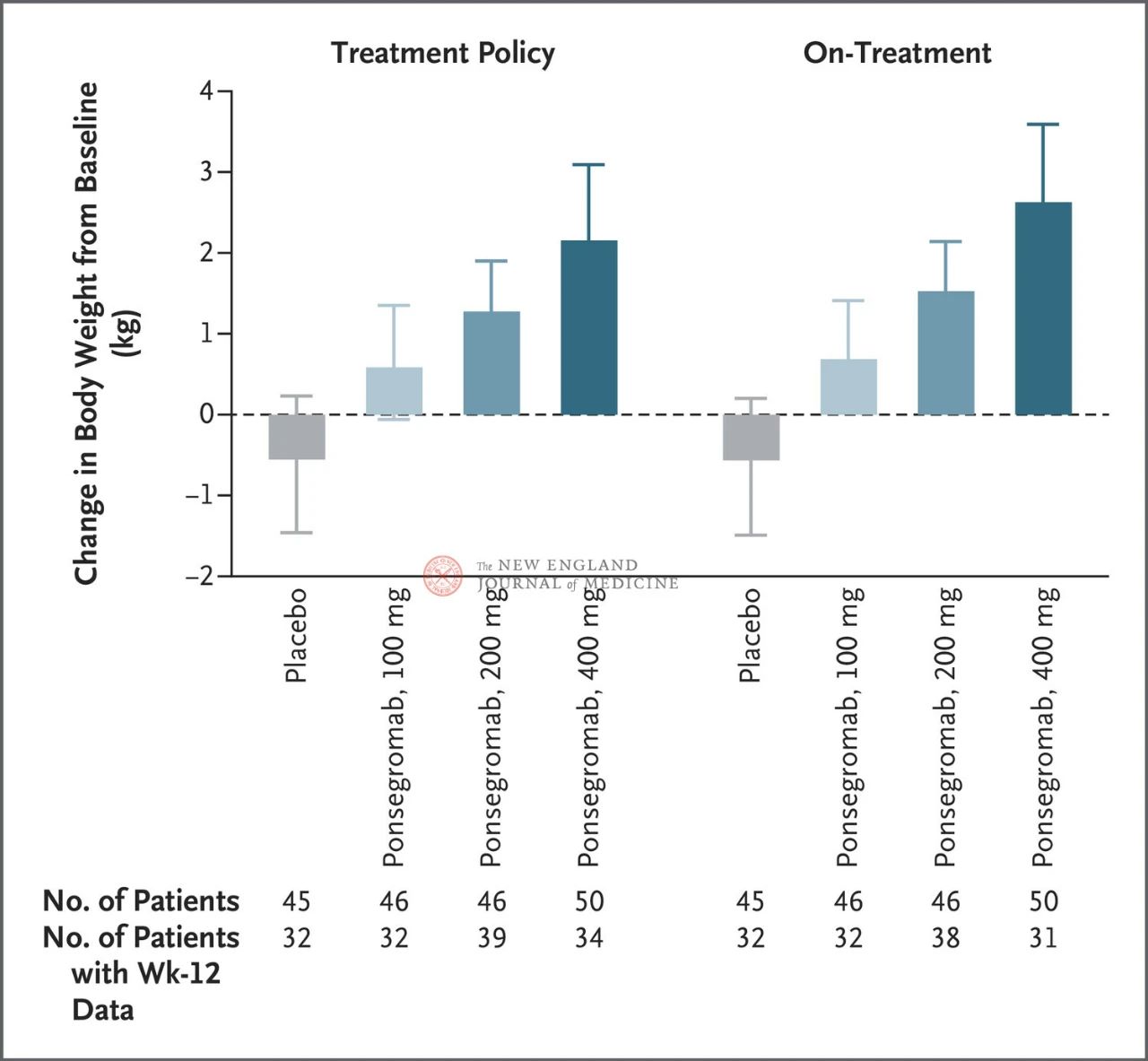
Celkem bylo 187 pacientů náhodně rozděleno do skupin, kterým byl ponsegromab podáván v dávce 100 mg (46 pacientů), 200 mg (46 pacientů), 400 mg (50 pacientů) nebo placebo (45 pacientů). Sedmdesát čtyři (40 procent) mělo nemalobuněčný karcinom plic, 59 (32 procent) rakovinu slinivky břišní a 54 (29 procent) kolorektální karcinom.
Rozdíly mezi skupinami se 100 mg, 200 mg a 400 mg a placebem byly 1,22 kg, 1,92 kg a 2,81 kg v uvedeném pořadí.
Obrázek ukazuje primární cílový parametr (změna tělesné hmotnosti od výchozího stavu do 12 týdnů) u pacientů s rakovinnou kachexií ve skupině s ponsegromabem a placebem. Po úpravě o konkurenční riziko úmrtí a dalších souběžných událostí, jako je přerušení léčby, byl primární cílový parametr analyzován stratifikovaným modelem Emax s použitím výsledků z 12. týdne z Bayesovské společné longitudinální analýzy (vlevo). Primární cílové parametry byly také analyzovány podobným způsobem s použitím odhadovaných cílů pro skutečnou léčbu, kde byla pozorování po všech souběžných událostech zkrácena (pravý obrázek). Intervaly spolehlivosti (uvedeny v článku
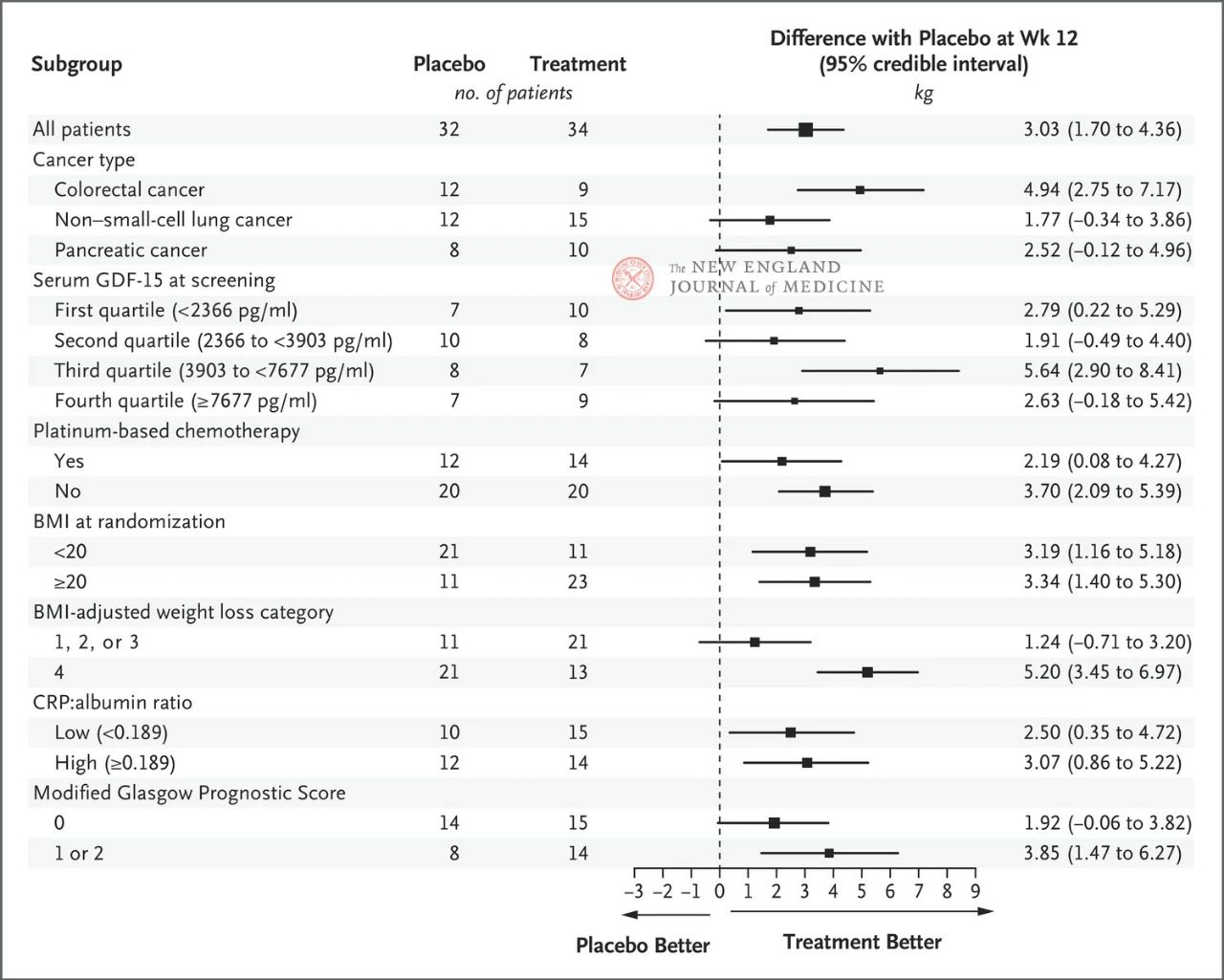
Účinek 400 mg ponsegromabu na tělesnou hmotnost byl konzistentní napříč hlavními přednastavenými podskupinami, včetně typu rakoviny, kvartilu hladiny GDF-15 v séru, expozice chemoterapii na bázi platiny, BMI a výchozího systémového zánětu. Změna hmotnosti byla konzistentní s inhibicí GDF-15 po 12 týdnech.
Výběr klíčových podskupin byl založen na post-hoc Bayesovské společné longitudinální analýze, která byla provedena po úpravě o kompetitivní riziko úmrtí na základě odhadovaného cíle léčebné strategie. Intervaly spolehlivosti by neměly být používány jako náhrada za testování hypotéz bez vícenásobných úprav. BMI představuje index tělesné hmotnosti, CRP představuje C-reaktivní protein a GDF-15 představuje faktor růstové diferenciace 15.
Na začátku studie neuváděl vyšší podíl pacientů ve skupině s ponsegromabem 200 mg žádné snížení chuti k jídlu; ve srovnání s placebem pacienti ve skupinách s ponsegromabem 100 mg a 400 mg hlásili zlepšení chuti k jídlu oproti výchozímu stavu po 12 týdnech, se zvýšením skóre FAACT-ACS o 4,12, respektive 4,5077. Mezi skupinou s dávkou 200 mg a skupinou s placebem nebyl zjištěn žádný významný rozdíl ve skóre FAACT-ACS.
Vzhledem k předem specifikovaným požadavkům na dobu nošení a problémům se zařízením poskytlo 59, respektive 68 pacientů údaje o změnách fyzické aktivity a cílových parametrech chůze v porovnání s výchozím stavem. U těchto pacientů došlo u pacientů ve skupině s dávkou 400 mg ve srovnání se skupinou s placebem ke zvýšení celkové aktivity po 12 týdnech, a to o 72 minut nárůstu nesedavé fyzické aktivity denně. Kromě toho došlo u skupiny s dávkou 400 mg ve 12. týdnu také ke zvýšení indexu bederního kosterního svalstva.
Výskyt nežádoucích účinků byl ve skupině s ponsegromabem 70 % ve srovnání s 80 % ve skupině s placebem a vyskytl se u 90 % pacientů, kteří současně dostávali systémovou protinádorovou léčbu. Výskyt nevolnosti a zvracení byl ve skupině s ponsegromabem nižší.
Čas zveřejnění: 5. října 2024